Węglan soduto biały bezwonny proszek lub cząsteczka w normalnej temperaturze. Charakteryzuje się wchłanianiem wody i stopniowo wchłania 1mol/l wody (około =15 procent ) z odsłoniętego powietrza. Jej hydraty to Na2CO3 · H2O, Na2CO3 · 7H2O i Na2CO3 · 10h2o. Węglan sodu jest łatwo rozpuszczalny w wodzie i glicerynie. W temperaturze 20 stopni można rozpuścić 20 g węglanu sodu w każdych 100 g wody, a maksymalna rozpuszczalność wynosi 35,4 stopnia. 49,7 g węglanu sodu można rozpuścić w 100 g wody, która jest słabo rozpuszczalna w absolutnym etanolu, ale słabo rozpuszczalna w propanolu.
Jego właściwości chemiczne są następujące:
Wodny roztwór węglanu sodu jest w pewnym stopniu alkaliczny i żrący. Może reagować z kwasami i niektórymi solami wapnia i baru. Roztwór ma odczyn zasadowy i może zmienić kolor na czerwony fenoloftaleiny.
(1) Stabilność - duża stabilność, ale może również rozkładać się w wysokiej temperaturze, tworząc tlenek sodu i dwutlenek węgla:
![]()
Długotrwała ekspozycja na powietrze może pochłaniać wilgoć i dwutlenek węgla z powietrza, generować wodorowęglan sodu i tworzyć twarde bloki:
![]()
Krystaliczny hydrat węglanu sodu (Na2CO3 · 10h2o) łatwo ulega wietrzeniu w suchym powietrzu:
![]()
(2) Funkcja termodynamiczna - funkcja termodynamiczna przy (298.15K, 100k):
Stan: półprzewodnikowy
Standardowa entalpia tworzenia mola: -1130.8 kJ · mol-1
Standardowa molowa energia swobodna tworzenia Gibbsa: -1048,1 kJ · mol-1
Entropia standardowa: 138,8 J · mol-1 · K-1
(3) Reakcja hydrolizy - podczas hydrolizy węglanu sodu w roztworze wodnym, zjonizowane jony węglanowe łączą się z jonami wodorowymi w wodzie, tworząc jony wodorowęglanowe, co powoduje redukcję jonów wodorowych w roztworze i pozostałych zjonizowanych jonów wodorotlenkowych, tak pH roztworu jest zasadowe.
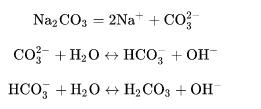
Ponieważ węglan może łączyć się z protonami (tj. jonami wodorowymi) w wodzie, tworząc wodorowęglan i kwas węglowy, i może łączyć się z protonami w kwasie, aby uwolnić dwutlenek węgla. Dlatego węglan sodu należy do zasady Bronsteda w kwasowo-zasadowej teorii protonów.
(4) Reakcja z kwasem - Weźmy jako przykład kwas solny. Gdy kwas chlorowodorowy jest wystarczający, powstają chlorek sodu i kwas węglowy, a niestabilny kwas węglowy jest natychmiast rozkładany na dwutlenek węgla i wodę. Ta reakcja może być wykorzystana do przygotowania dwutlenku węgla:
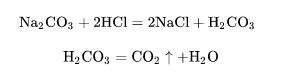
Ogólne równanie chemiczne to:
![]()
Gdy kwas solny jest mały, zachodzą następujące reakcje:
![]()
Węglan sodu może reagować podobnie z innymi rodzajami kwasów.
(5) Reakcja z alkaliami – węglan sodu może ulegać podwójnemu rozkładowi z alkaliami, takimi jak wodorotlenek wapnia i wodorotlenek baru, w celu wytrącenia osadu i wodorotlenku sodu. Ta reakcja jest powszechnie stosowana w przemyśle do przygotowania sody kaustycznej (powszechnie znanej jako kaustyzacja):
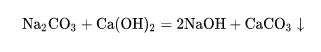
(6) Reakcja z solą
Węglan sodu może ulegać podwójnemu rozkładowi z solą wapnia i solą baru, tworząc strącanie i nową sól sodową:
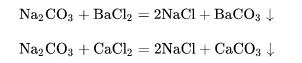
Ponieważ węglan sodu jest hydrolizowany w wodzie w celu wytworzenia wodorotlenku sodu i kwasu węglowego, jego reakcja z niektórymi solami popchnie równowagę chemiczną w pozytywnym kierunku, aby wygenerować odpowiednie zasady i dwutlenek węgla:
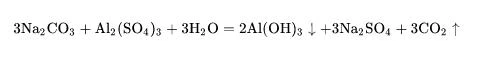
Podsumowując, posiada wiele właściwości chemicznych, co również determinuje szerokie spektrum jego zastosowań. Węglan sodu jest jednym z ważnych surowców chemicznych. Znajduje szerokie zastosowanie w przemyśle lekkim, codziennym przemyśle chemicznym, materiałach budowlanych, przemyśle chemicznym, spożywczym, metalurgicznym, tekstylnym, naftowym, obronie narodowej, medycynie i innych dziedzinach. Jest również używany jako surowiec, środek czyszczący i detergent do produkcji innych chemikaliów, a także fotografii i analiz. Za nimi podążają przemysł metalurgiczny, włókienniczy, naftowy, obronny, medyczny i inne. Przemysł szklarski jest największym konsumentem sody kalcynowanej, zużywając 0.2T sody kalcynowanej na tonę szkła. Stosowany jest głównie do szkła float, powłoki szklanej kineskopu, szkła optycznego itp. Wśród przemysłowej sody kalcynowanej, przemysłu lekkiego, przemysłu materiałów budowlanych i przemysłu chemicznego około 2/3, a następnie metalurgii, tekstyliów, ropy naftowej, obrony narodowej, medycyny i innych gałęziach przemysłu.. Stosowany w przemyśle chemicznym, metalurgii itp. Zastosowanie ciężkiej sody kalcynowanej może zmniejszyć lot pyłu alkalicznego, zmniejszyć zużycie surowców, poprawić warunki pracy, poprawić jakość produktu, zmniejszyć erozję alkaliów proszkować na materiały ogniotrwałe i przedłużać żywotność pieców. Jako bufor, neutralizator i polepszacz ciasta może być stosowany w ciastach i produktach mącznych oraz może być stosowany w odpowiedniej ilości w zależności od potrzeb produkcyjnych.
Rozwój węglanu sodu jest również bardzo duży, głównie odnosząc się do rozwoju metody produkcji sody z naturalnych alkaliów: ① już w 1849 roku pionierzy znaleźli wodorowęglan sodu w rzece słodkiej wody w Wyoming w USA i używali go do prania i farmacji . W 1905 roku przeprowadzono pierwszą próbną produkcję sody kalcynowanej przy użyciu naturalnej sody z Lake Sears w Kalifornii. W 1938 roku, kiedy amerykańska firma dostarczająca paliwo Intermountain poszukiwała ropy i gazu w dorzeczu rzeki Green w stanie Wyoming, odkryła największe na świecie naturalne złoże alkaliczne bogate w węglan sodu. W 1976 roku soda kalcynowana produkowana przez naturalne zasady w Stanach Zjednoczonych stanowiła 70 procent całkowitej produkcji, aw 1982 roku 94% całkowitej produkcji, przy rocznej zdolności produkcyjnej 9,5 mln ton. ② Od lat 60. Związek Radziecki przetwarzał tlenek glinu za pomocą nefelinu (naturalny kamień alkaliczny zawierający tlenki sodu, potasu, glinu i krzemu) i jednocześnie produkował sodę kalcynowaną, potaż i cement, realizując uprzemysłowienie, dzięki czemu surowce nefelinowe mogą być wszechstronnie wykorzystywane bez odprowadzanie odpadów. Do 1975 roku powstało pięć zakładów przetwórstwa nefelinu.

